1. 最新の作業の進捗状況:
天然パクリタキセルの規制上の宣言:
● 中国 CDE:
2021 年 12 月 13 日に、CDE 追加申請が完了しました (最新の CDE 状況は写真に示されています)。そしてHandeは、2022年1月18日から20日にかけて雲南省食品医薬品監督管理局のGMP現場実地検査を受け入れた。CDEは今後、APIの登録および変更審査のための承認文書を発行しないため、APIの登録および変更審査に関するいかなる裏付け文書も発行しない。現時点では、準備とデバイスによってすでに参照できます。CDE の承認に従って、関連するプロセスと標準の変更については、変更通知メールを参照してください。。
立ち入り検査後、雲南ハンデは中国市場での商業販売を正式に再開する。貴社では研究開発、小規模テスト、パイロットテスト、臨床用途などニーズに合わせてHandeの製品をご利用いただけます。申請資料は Hande CDE 資料を直接引用できます。
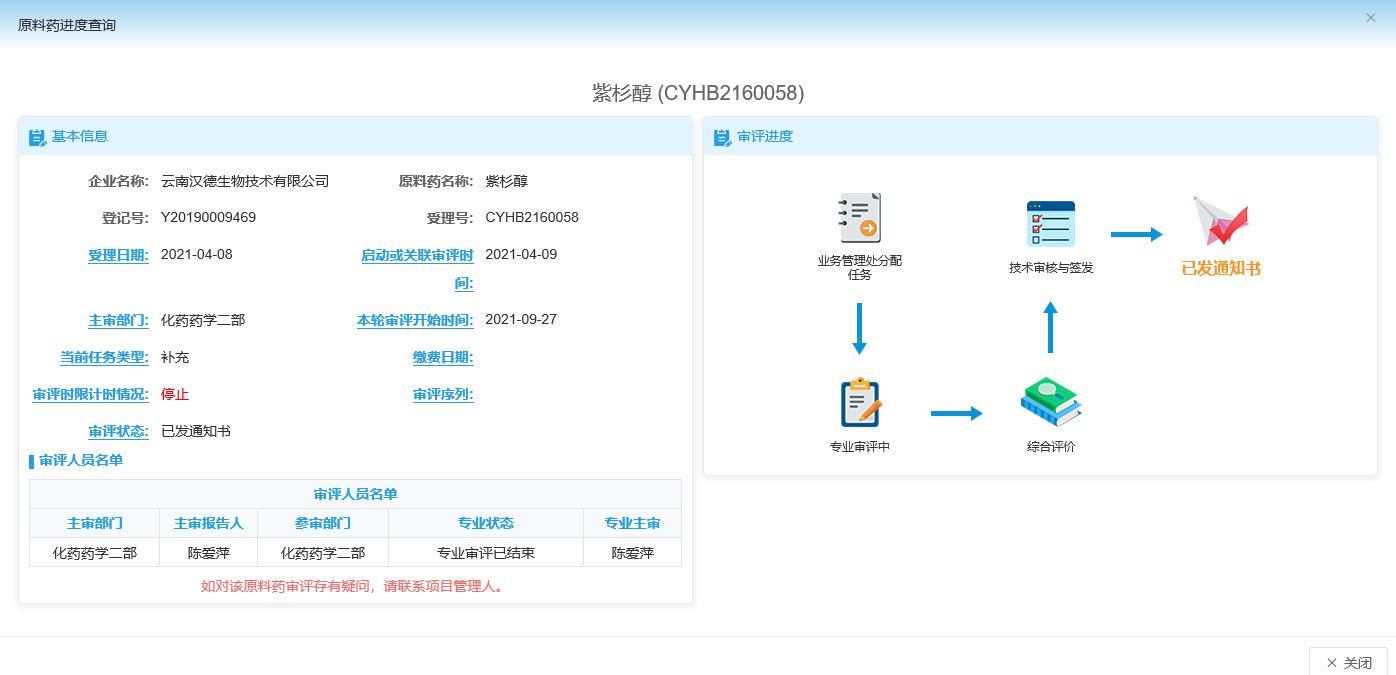
● EU EDQM:
Hande は CEP 証明書と「EU への API の輸出に関する証明書文書」(以下「WC」)を取得し、EU 市場での正式な商業販売が再開されました。あなたの会社がCEP証明書と認可レターまたは製品を必要とする場合は、時間内にご連絡ください。
● 米国 FDA:
DMF変更情報が送信されました。
● その他の国または地域:
ロシア: 既存の顧客は登録をアクティブ化し始めています。
インド: DMF データが提出されました。
ブラジル: DMF データ準備。
日本: 登録資料は提出済み。
オーストラリアの TGA: 準備中。
EU GMP: 準備中。
残りの国も同時に申請します。将来的には、Hande は貴社の国際戦略市場の拡大を支援します。
2. 10-DAB 半合成パクリタキセル生産ライン:
パイロット生産は終了し、テストは完了しました。現在、品質調査と安定性検査を実施しています。3バッチ検証バッチ生産計画は、装置の設置と試運転が完了した後、2022年1月に開始されます。
10-DAB 半合成パクリタキセルの規制当局への登録計画:
● 中国 CDE: 文書番号: Y20210000685、2022 年の第 2 四半期に申請を開始する予定です。
● EDQM と FDA: 2022 年の第 4 四半期に申請する予定。
3.一次加工ライン:
複数のイチイ植栽基地の現場統計とサンプリング試験を通じて、有効量のパクリタキセルの十分な原料供給を確保するために、3つの大規模植林基地で年間調達計画が実施されています。10-DABの年間生産量は2000kg/年で、安定した品質と長期供給が可能です。
● 10-DAB III 規制当局への申請:
DMF:DMF番号を取得しました。
2. その他の情報
1. 感染症の影響により、ハンデはCPHI展示会に参加しなくなりました。貴社へのより良いサービスを提供するために、私たちは今後も顧客訪問を実施し、より良いサービスで貴社の市場開拓業務に協力していきます。
投稿日時: 2022 年 2 月 18 日